

治療目的/所見クラスⅠ クラスⅡa クラスⅡb
二次予防
◦心停止,SVT,またはVF ICD
運動制限
アミオダロン
一次予防
◦リスク因子*を複数有する運動制限ICD,アミオダロン
◦リスク因子*が1つある運動制限ICD
二次予防
◦心停止,SVT,またはVF ICD
運動制限
アミオダロン
一次予防
◦リスク因子*を複数有する運動制限ICD,アミオダロン
◦リスク因子*が1つある運動制限ICD
5 肥大型心筋症(HCM)
本症は心筋の異常肥大を来たす原因不明の疾患で334),335),病因として心筋βミオシン重鎖,心筋トロポニンT,心筋ミオシン結合蛋白Cなどのサルコメア
蛋白をコードする遺伝子の変異が同定されている336).年間死亡率は1~ 2%と報告されている173),337)-340).本症の死因の過半数が突然死で,特に若年
者の突然死の原因として重要である.心停止からの蘇生例や持続性心室頻拍は突然死の高リスク群で,二次予防のためにICDが適応となる341)-344).
臨床像からは,繰り返す失神発作(特に小児で運動中に発生する失神)は,心事故の危険性が高い148),338),340).しかし,幸いこのような重篤な失神発作
を示す例は我が国では比較的少ない173).一親等以内あるいは複数の突然死の家族歴があると突然死の危険が高くなる145),148),338),344),346).
ホルター心電図で検討すると,90%になんらかの心室性不整脈を認め,200個/日以上の心室期外収縮は20%,2連発は約40%,非持続性心室頻拍は
17~28%に認められる347)-352).心室期外収縮を突然死の危険因子とする報告はほとんどないが,非持続性心室頻拍を突然死の独立した危険因子とする
報告が多い345),348),351),353)-355).感度,特異度はいずれも70%前後で陰性的中率は95%以上と高く345),348),351),突然死危険群の層別化に
有用と考えられる.ただし,陽性的中率は20~25%と低く,非持続性心室頻拍を認めても必ずしも突然死を来たさない.有症候例や家族歴を有するHCMを
多く含む施設の検討では,非持続性心室頻拍がないと年間死亡率が約1%で,家族歴があると8~ 9%と有意に高くなる348),352),356),357).無症候例を多く
含む一般のHCMでは,非持続性心室頻拍の有無で予後に差はないとされている349),358),359).
心エコー図における著明な左室壁肥厚(最大壁厚30mm以上)も突然死の危険因子となる182),338),360)-362).左室流出路狭窄例でも突然死は高率であ
るが338),363),陽性的中率は低い.心尖部肥大型では突然死の危険は少ないと考えられていたが,心筋病変が進行した例では突然死も発生する364),365).
運動負荷試験中の収縮期血圧低下または上昇不良(20mmHg以下)はHCMの約25%にみられ,若年例や中年例(50歳以下)では突然死の危険因子と
なる173)-175),366).
電気生理検査はHCMの突然死の予知に有用かどうかは確認されていない145),146),346)-348),367)-369).HCMの突然死のリスクは遺伝子異常の種類に
より異なるが335),370)-376),十分な検索が行われたとはいえず,かつ検査は一部の研究機関に限られることから,まだ突然死予知の有用な方法とはいえな
い.
最近のICDの成績では,原因不明の失神,突然死の家族歴,ホルター心電図でのNSVT,著明な左室壁肥厚(≧30mm)のいずれか1つでもあれば,
2 つまたはそれ以上と同等のICD作動が認められている344)(表7).我が国でも高危険群では,ICDが考慮されることになる.
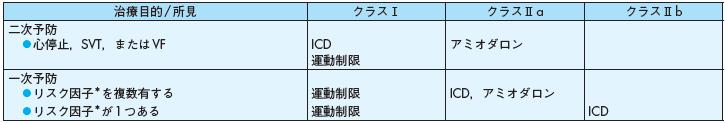
表7 肥大型心筋症(HCM)における突然死予防
* 原因不明の失神発作,突然死の家族歴,ホルター心電図での頻回(5回/日以上)あるいは連発数の多い(10連発以上)NSVT,
著明な左室壁肥厚(≧ 30mm),運動中の血圧上昇不良(<20mmHg)または低下
著明な左室壁肥厚(≧ 30mm),運動中の血圧上昇不良(<20mmHg)または低下
心臓突然死の予知と予防法のガイドライン(2010年改訂版)
Guidelines for Risks and Prevention of Sudden Cardiac Death(JCS 2010)
Guidelines for Risks and Prevention of Sudden Cardiac Death(JCS 2010)