

治療目的/所見クラスⅠ クラスⅡa クラスⅡb
二次予防
◦SIDSの蘇生例でQTc ≧440msec ICD*
+β遮断薬
一次予防
◦前子がSIDSで死亡し,かつQTc ≧440msec ICD*
+β遮断薬
◦家族歴がなくQTc ≧440msec β遮断薬
二次予防
◦SIDSの蘇生例でQTc ≧440msec ICD*
+β遮断薬
一次予防
◦前子がSIDSで死亡し,かつQTc ≧440msec ICD*
+β遮断薬
◦家族歴がなくQTc ≧440msec β遮断薬
治療目的/所見クラスⅠ クラスⅡa クラスⅡb一次予防
◦カルニチン輸送異常症
◦CPT- Ⅱ欠損症
◦CA translocase欠損症
◦LCAD欠損症
◦VLCAD欠損症
◦ LCHAD/三頭酵素欠損症(共通予防法として下記)
頻回の高炭水化物低脂肪食,長鎖脂肪酸摂取を控え中鎖脂肪酸を取る,
L‐カルニチンL‐カルニチンL‐カルニチン
◦カルニチン輸送異常症
◦CPT- Ⅱ欠損症
◦CA translocase欠損症
◦LCAD欠損症
◦VLCAD欠損症
◦ LCHAD/三頭酵素欠損症(共通予防法として下記)
頻回の高炭水化物低脂肪食,長鎖脂肪酸摂取を控え中鎖脂肪酸を取る,
L‐カルニチンL‐カルニチンL‐カルニチン
治療目的/所見クラスⅠ クラスⅡa クラスⅡb
二次予防
◦蘇生例ペースメーカ
一次予防
◦家族性の刺激伝導系異常ペースメーカ
二次予防
◦蘇生例ペースメーカ
一次予防
◦家族性の刺激伝導系異常ペースメーカ
1 乳幼児突然死症候群(Sudden Infant Death Syndrome:SIDS)
SIDSはいまだその原因が明確ではなく,多因子説が唱えられている.しかし近年,不整脈が原因とするいくつかの説が挙げられている.
(1)QT 延長症候群(LQTS)
34,442名の新生児の心電図を生後1 週以内で記録し,1 年後の生存の有無を確認し,突然死とQT延長の関係を検討した報告がある520).SIDS24 例の
QTc は435±45msecで,これは生存例(400± 20msec)およびSIDS以外の死亡例(393± 24msec)に比べ,有意に大であった.さらにSIDS24 例中12例で
QTc が440msec以上であり,SIDS以外で死亡した例はすべてQTc が440msec未満であった.このことから,QTc ≧ 440msec以上の新生児ではSIDSを
起こす危険性が高いといえる(表17).QTc は生後2か月までは延長し,その後6か月までに出生時の値に戻るとされている521).このことはSIDSが生後
1か月以内では少なく,2~ 3か月で多くなり,4か月以後に減少するという所見と一致する.また,89例のapparent life-threatening event(ALTE)における
心電図の検討では,QT dispersionはSIDS群で0.0318± 0.020secとコントロール群の0.026±0.017secに比較して有意に大であった522).このような心電図
によるスクリーニングは有用と思われるが,費用対効果も問題になる523).新生児期では,QTc ≧ 440msecはSIDSの予測に有用で,QT dispersionの延
長はやや有用と考えられる.
近年,SIDS症例における遺伝子解析により,多くの遺伝子異常が発見されており524)-528),SIDSではLQTSは重要な原因と1 つとして考えられるように
なってきている.
(2)SCN5A 遺伝子異常
93例のSIDS死亡児の遺伝子検索で,2例にSCN5Aの異常が検出され203)-205),SCN5Aの異常とSIDSとの関係を推測させる.
(3)RyR2 遺伝子異常
RyR2遺伝子異常によるSIDSも報告されている529).
(4)刺激伝導系異常
SIDS例の剖検例の検討では,束枝心室間伝導路が有意に多いことが報告されている530).この他,房室結節動脈の線維筋性異形成,ヒス束内出血,
心筋炎,刺激伝導系へのリンパ球浸潤,心内膜線維弾性症例での左脚の線維化なども認められる.心室中隔欠損に合併した房室ブロックによる幼児突然
死の報告もある531).ただし,このような刺激伝導系の生前の予知は困難である.治療はペースメーカが中心となる(表18).
(5)脂肪酸代謝異常
ミトコンドリアにおける脂肪酸のβ酸化障害により,長鎖アシルカルニチン(acylcarnitine)などが蓄積することにより,心室頻拍,心房頻拍,洞機能不全,
房室ブロック, 左脚ブロックなどの心電図異常を来たし,SIDSをもたらすとの報告がある532).低血糖,酸血症に種々の不整脈,伝導障害を合併する症例で
は,ガスリー法によるアシルカルニチンの測定が診断に有用である.治療は食事療法が中心である(表19).
(6)その他
SIDSの死因に徐脈や無呼吸が関係していることが報告されている533).また,呼吸運動,心電図,パルスオキシメータなどによるモニタリングを行うと,
未熟児やALTE例に徐脈や無呼吸が多いことが報告されている534)-536).一度徐脈が記録がされた児では,徐脈が繰り返し記録される例が多く,
モニターで正常であった例がその後に徐脈となることは少ない535),536).新生児期に徐脈や無呼吸などを認めた場合には,家庭モニタリングがSIDSの
予防に有効と思われる.
表18 乳幼児突然死症候群(SIDS)における突然死予防(刺激伝導系の異常)
表19 乳幼児突然死症候群(SIDS)における突然死予防(脂肪酸代謝異常)
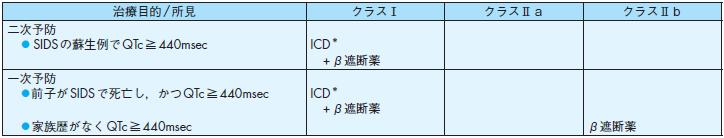
表17 乳幼児突然死症候群(SIDS)における突然死予防(QT延長症候群)
*乳幼児での植込み型除細動器による治療は困難を伴う.


CPT-Ⅱ:carnitine palmitoyltransferase type Ⅱ,CA translocase:carnitine-acylcarnitine translocase,LCAD:long-chain acyl-coenzyme
A dehydrogenase,VLCAD:very-long-chain acyl-coenzyme A dehydrogenase,LCHAD:long-chain 3-hydroxyacyl-coenzyme A
dehydrogenase
A dehydrogenase,VLCAD:very-long-chain acyl-coenzyme A dehydrogenase,LCHAD:long-chain 3-hydroxyacyl-coenzyme A
dehydrogenase
- Home
- Ⅴ 小児における突然死
- 2 突然死を来たす主な病態・疾患
- 1 乳幼児突然死症候群(Sudden Infant Death Syndrome:SIDS)
心臓突然死の予知と予防法のガイドライン(2010年改訂版)
Guidelines for Risks and Prevention of Sudden Cardiac Death(JCS 2010)
Guidelines for Risks and Prevention of Sudden Cardiac Death(JCS 2010)